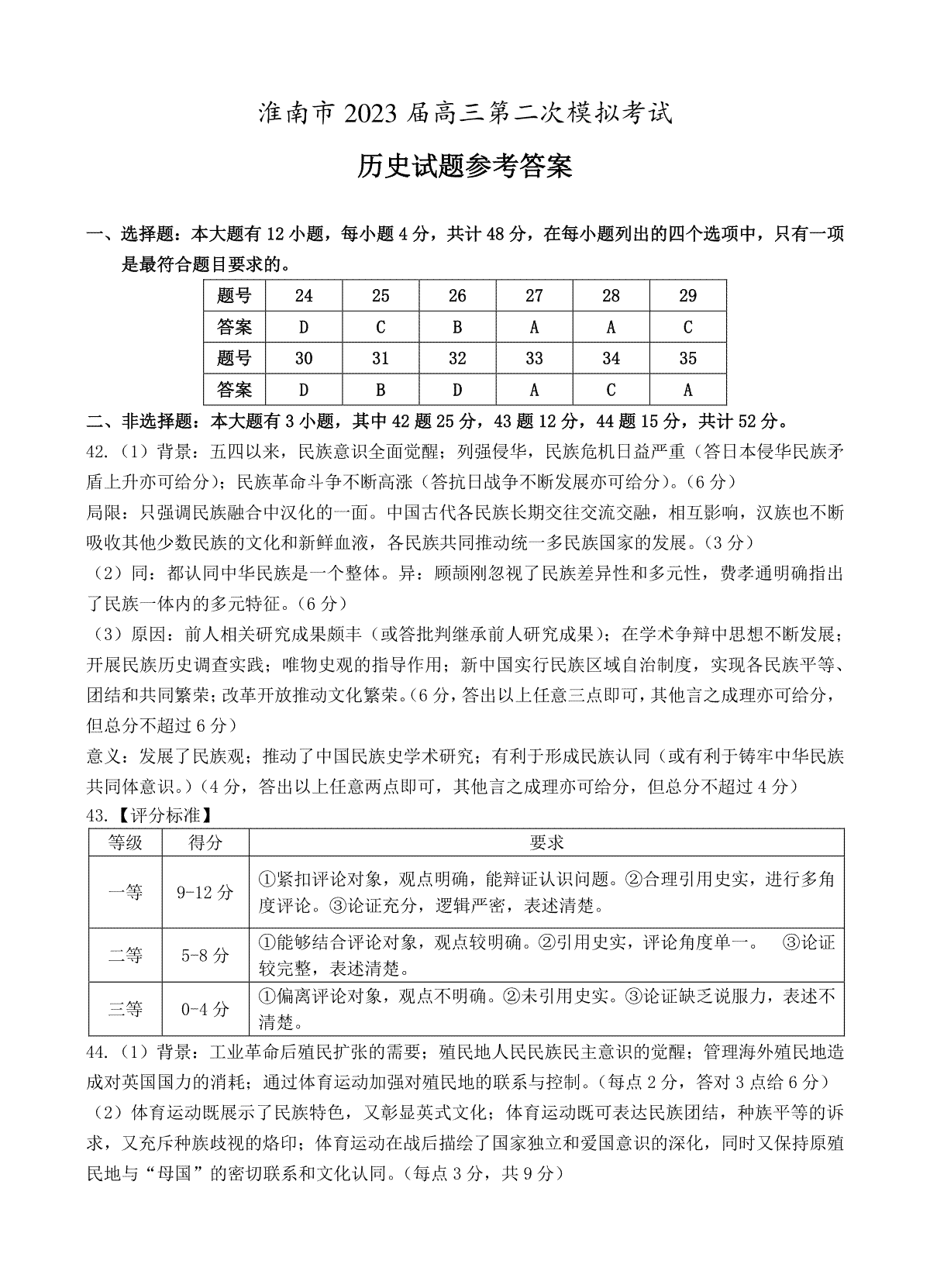
nacl电离方程式
2020-07-18阴极反应:2Cl-(氯离子)-2e=Cl2↑()阳极反应:2H+(氢离子)+2e = H₂↑ (氢气)总反应:2NaCl +2H₂O==2NaOH+H₂↑+Cl₂↑ 在阳极氯离子被氧化生成,在阴极氢离子被还原生成氢气,因为氢离子被消耗促进水的电离产生更多的氢氧根,故可看作生成了NaOH。

氯化钠的晶体形成立体对称。其晶体结构中,较大的氯离子排成立方最密堆积,较小的钠离子则填充氯离子之间的八面体的空隙。每个离子周围都被六个其他的离子包围着。这种结构也存在于其他很多化合物中,称为氯化钠型结构或石盐结构。
1.电解熔融态氯化钠制取金属钠:
2.电解食盐水:
3.与硝酸银反应:离子方程式:(其实质为Cl-的性质)
4.与浓硫酸反应(实验室制氯化氢) NaCl的检验一:向氯化钠溶液中滴入硝酸酸化过的硝酸银溶液,有白色沉淀(氯化银沉淀)产生,证明有Cl-。二:用铂丝蘸取少量溶液,置于酒精灯上灼烧,火焰呈黄色,可证含有Na+。三:为了消除干扰,可取原试液加饱和氢氧化钡至呈明显碱性,这时大部分阳离子和PO₄3−、AsO43−等阴离子都将被沉淀。引入试液中的Ba2+应继以碳酸铵除之,最后用灼烧法除去铵盐。残渣用水加热浸取后,取溶液以HAc酸化,按1:8的滴数加乙酸铀酰锌试剂,并用玻璃棒摩擦管壁,如有柠檬黄色结晶形沉淀生成,示有Na+存在。